Kinecteen
| Kinecteen | |
|---|---|
| |
| Wirkstoff | Methylphenidathydrochlorid |
| Verfügbare Dosierungen |
|
| Darreichungsform | Tablette (nicht teilbar) mit veränderter Wirkstofffreisetzung |
| Wirkmechanismus | Dopamin-Wiederaufnahmehemmer (DRI) |
| Hersteller | MEDICE Arzneimittel Pütter |
Kinecteen ist ein seit April 2017 in Deutschland erhältliches Retardpräparat mit dem Wirkstoff Methylphenidat. Unter Verweis auf ein Review von Banaschewski et al.[1] gibt der Hersteller MEDICE Arzneimittel Pütter eine Wirkdauer von bis zu zwölf Stunden an. Eine zweite Einnahme im Tagesverlauf soll so entfallen. Kinecteen stellt daher ein direktes Konkurrenzprodukt zu Concerta dar.
Kinecteen unterliegt dem Betäubungsmittelgesetz. Es kann ADHS-diagnostizierten Kindern und Jugendlichen von 6 bis 18 Jahren sowie seit 2023 auch initial Erwachsenen Patienten rezeptiert werden.[2]
Verfügbare Dosierungen
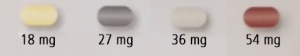
Die vier verfügbaren Dosierungen sind durch verschiedene Tablettenfärbungen gekennzeichnet. Dabei handelt es sich um eine MEDICE-typische Hinweismarkierung, die sich in einem ähnlichen Stufenmuster auch bei der Medikinet-Gruppe wiederfindet. Kinecteen ist in folgenden Dosierungen erhältlich (siehe Tabelle):
| Dosierung | Entsprechung | Färbung | Verfügbare Packungsgröße(n) |
|---|---|---|---|
| 18 mg Methylphenidathydrochlorid | 15,6 mg Methylphenidat | Beige | 28 Stück (12448964) |
| 27 mg Methylphenidathydrochlorid | 23,3 mg Methylphenidat | Grau | 28 Stück (12448970) |
| 36 mg Methylphenidathydrochlorid | 31,1 mg Methylphenidat | Weiß | 28 Stück (12448993) |
| 54 mg Methylphenidathydrochlorid | 46,7 mg Methylphenidat | Rot | 28 Stück (12449018) |
Erstattungsfähigeit
Kinecteen ist in Deutschland sowohl für Kinder und Jugendliche als auch für Erwachsene voll erstattungsfähig.[3]
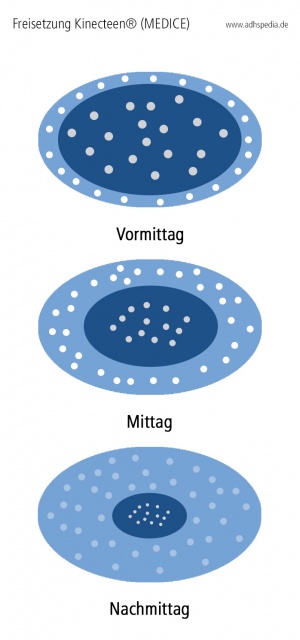
Galenik und Freisetzungsmechanismus
Bei Kinecteen ist Methylphenidathydrochlorid in eine hydrophile, langsam erodierende Retardmatrix eingebettet. Nach Einnahme dringt Flüssigkeit aus dem Gastrointestinaltrakt in die Tablette ein, die Matrix quillt auf und bildet eine viskose Gelschicht, aus der der Wirkstoff vor allem durch Diffusion und die allmähliche Erosion der Matrix freigesetzt wird.[4][5] Dieser Freisetzungsmechanismus soll eine über viele Stunden relativ gleichmäßige systemische Verfügbarkeit von Methylphenidat ermöglichen. Der Hersteller gibt in Anlehnung an Daten zu lang wirksamen Stimulanzien eine Wirkdauer von bis zu zwölf Stunden an, sodass in der Regel eine einmal tägliche Morgengabe ausreicht.[6][7]
Unsachgemäße Verwendung und Eignung zum Missbrauch
Die Retardtabletten von Kinecteen müssen im Ganzen mit Flüssigkeit eingenommen werden und dürfen nicht geteilt, zerkaut oder zerstoßen werden, da eine mechanische Zerstörung der Matrix den Retardmechanismus aufhebt und zu einer raschen Freisetzung der gesamten Dosis mit erhöhtem Risiko akuter Überdosierungserscheinungen führen kann.[8][9][10] Das Präparat gilt in dieser Darreichungsform als wenig geeignet, um einen raschen stimulierenden Effekt zu erzielen, da die Freisetzung explizit auf eine langsam ansteigende und über Stunden anhaltende Wirkstoffspiegelbildung ausgelegt ist und eine Manipulation der Tablettenformulation als Missbrauch angesehen wird.[11][12] Eine missbräuchliche Applikation zerkleinerter Tabletten etwa durch nasale oder intravenöse Anwendung ist potenziell hochgefährlich, da unlösliche Hilfsstoffe wie Talkum zu Partikelembolien in der Lungenstrombahn führen können und in Fallberichten mit lebensbedrohlicher pulmonaler Talcose und tödlichen Embolien in Verbindung gebracht werden.[13][14][15]
Besonderheiten und Hinweise zur Einnahme
Ausführliche Angaben zu möglichen Nebenwirkungen sind im Artikel Methylphenidat zu finden.
Einnahmezeitpunkt
Aufgrund der langen Wirkdauer von maximal zwölf Stunden muss das Präparat am frühen Morgen (vor Schulbeginn) eingenommen werden. Eine spätere Einnahme kann Einschlafstörungen zur Folge haben. Ist ein späterer Wirkungseintritt gewünscht, zum Beispiel an Wochenenden oder während der Schulferien, kann an diesen Tagen auf ein kürzer wirkendes Präparat ausgewichen werden.
Nahrungsmittelabhängigkeit
Die Einnahme von Kinecteen kann unabhängig von einer Frühstücksmahlzeit erfolgen.
Allergikereignung
Kinecteen enthält Lactose und kann daher für Patienten mit entsprechenden Unverträglichkeiten ungeeignet sein.
Sonstiges
MEDICE Österreich ließ die Wortmarke Kinecteen im November 2016 in der Europäischen Union registrieren.[16] Die Entwicklung des Medikaments fand in Israel statt.
Weblinks
- Informationen zu Kinecteen in der Gelben Liste
Weitere interessante Artikel

Einzelnachweise
- ↑ https://www.ncbi.nlm.nih.gov/pubmed/16680409
- ↑ https://www.aerztezeitung.de/Medizin/Neue-Option-zum-Therapiestart-bei-Erwachsenen-mit-ADHS-444795.html?noGatewayCall=1
- ↑ https://www.aerztezeitung.de/Medizin/Neue-Option-zum-Therapiestart-bei-Erwachsenen-mit-ADHS-444795.html?noGatewayCall=1
- ↑ Goldoozian S, et al. Gel Strength of Hydrophilic Matrix Tablets in Terms of In Vitro Robustness. AAPS PharmSciTech. 2021;22(8).
- ↑ Wheless JW. A clinician’s guide to oral extended-release drug delivery. Innov Clin Neurosci. 2018;15(1–2):25–35.
- ↑ Kinecteen. ADHSpedia, abgerufen am 24. November 2025.
- ↑ Banaschewski T, et al. Long-acting medications for the hyperkinetic disorders. Eur Child Adolesc Psychiatry. 2006;15(8):476–495.
- ↑ Fachinformation Kinecteen Retardtabletten. Medice Arzneimittel, Stand 2023.
- ↑ Beipackzettel Kinecteen 27 mg Retardtabletten. Apotheken Umschau, abgerufen am 24. November 2025.
- ↑ Nguyen VT et al. Pulmonary effects of IV injection of crushed oral tablets. AJR American Journal of Roentgenology 2015.
- ↑ Ward S et al. Talcosis associated with IV abuse of oral medications. AJR American Journal of Roentgenology 2000.
- ↑ Stoops WW et al. Safety and efficacy considerations due to misuse of extended release formulations of stimulant medications. In Drug and Alcohol Dependence 2010.
- ↑ Hill AD et al. Talc lung in a drug abuser. Thorax 1990.
- ↑ Ranib M et al. Pulmonary intravascular talcosis due to intravenous drug abuse of oral medications. SAS Journal of Medicine 2021.
- ↑ Patel J et al. Fatal pulmonary embolism due to intravenous injection of oral opiate tablets. Society of Hospital Medicine Abstracts 2020.
- ↑ http://trademark.markify.com/trademarks/ctm/kinecteen/016042293

